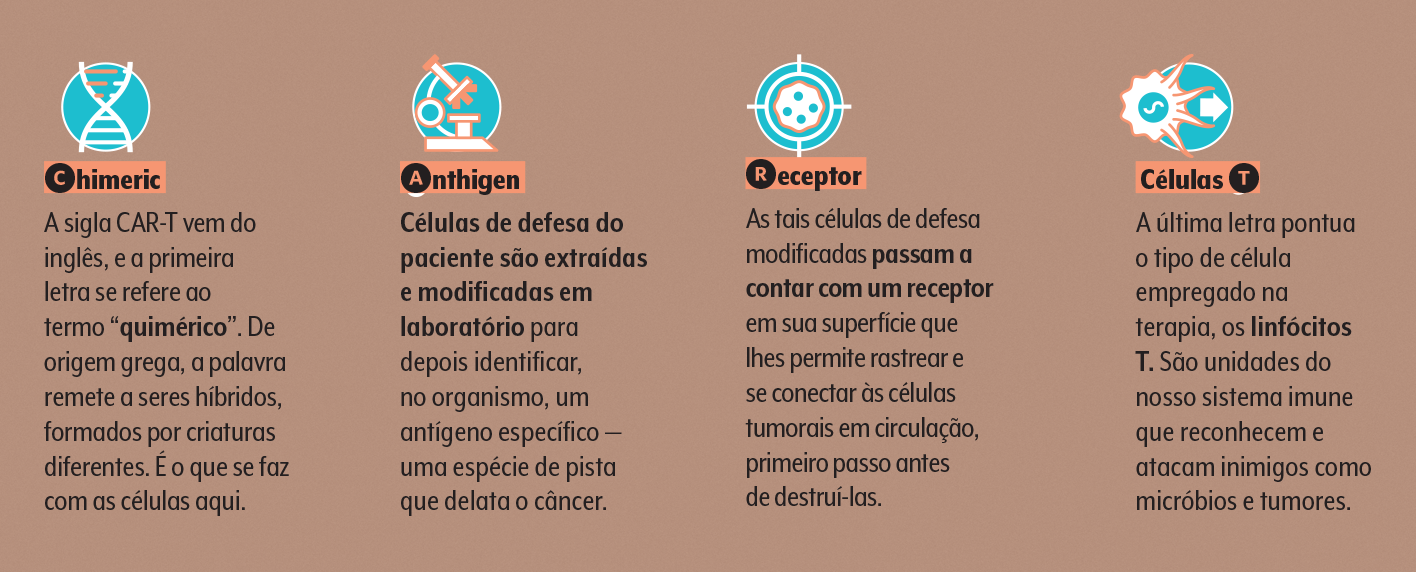
“Remédios vivos”: é assim que o imunologista americano Carl June, um dos pioneiros no estudo da terapia celular contra o câncer, define a nova classe de tratamento que ficou famosa pela sigla CAR-T.
A bem da verdade, não falamos de medicamentos no sentido convencional, mas de células de defesa extraídas do próprio paciente, modificadas geneticamente em laboratório e reintroduzidas no corpo para armar uma caçada às células tumorais.
Por enquanto, não é qualquer câncer que está na mira das CAR-T. Essa estratégia totalmente personalizada já foi aprovada para uso comercial, inclusive no Brasil, para alguns tipos de leucemia, linfoma e mieloma múltiplo, todos eles tumores que nascem e se espalham no sangue.
“A grande beleza desse tratamento é infundir só uma vez no paciente células que irão atuar no organismo talvez até mais de dez anos, impedindo que a doença volte”, diz o hematologista Vanderson Rocha, professor titular da Faculdade de Medicina da Universidade de São Paulo (USP) e o único médico brasileiro a acompanhar in loco o último Congresso Europeu de CAR-T Cell, realizado em fevereiro no frio de Roterdã, na Holanda.
VEJA SAÚDE também esteve lá, registrando os progressos e os complexos debates que envolvem uma área da medicina frequentemente associada ao adjetivo “revolucionário”.
Outro que marcou presença, em carne e osso, foi o professor June, da Universidade da Pensilvânia (EUA). Ele foi o responsável pela primeira aplicação de CAR-T numa criança no mundo — à época em caráter de pesquisa.
Emily Whitehead foi submetida ao tratamento em 2012 quando tinha 6 anos de idade. Está há mais de uma década livre da leucemia linfoblástica aguda que poderia ter ceifado sua vida.
O tratamento, desenvolvido em parceria com a Novartis e hoje comercializado por ela, foi autorizado para uso nos EUA em 2017 e, por aqui, em 2022.
Um dos poucos brasileiros a compartilhar a sorte de Emily é o médico recém-formado Lucas Visconti, de Valença (RJ). Seu destino se cruzou com o do professor Rocha, da USP, e o rapaz, então com 26 anos, passou por uma terapia CAR-T experimental e 100% nacional criada pelo Hemocentro e a USP de Ribeirão Preto. Em maio, ele completa um ano sem resquícios de uma leucemia.
Tanto Lucas cá como Emily lá não partiram para o novo procedimento logo de cara, após o diagnóstico. Só chegaram a ele depois de as medicações tradicionais falharem.
“Hoje as CAR-T são indicadas, no geral, a pacientes cuja doença é resistente ou retornou após duas linhas de tratamento”, esclarece a hematologista Lucila Kerbauy, do Hospital Israelita Albert Einstein, em São Paulo.
“Antes disso, podemos lançar mão de quimioterapia, terapia-alvo, imunoterapia e o transplante de medula, por vezes com proposta curativa”, completa a médica. Se essas táticas não funcionarem, pelo menos até o momento, aí podem ser recrutadas as CAR-T.
No Brasil, fora as versões elaboradas por universidades e centros de pesquisa (ainda não liberadas para uso comercial), temos três terapias aprovadas pela Anvisa para tipos específicos de leucemia, linfoma e mieloma, quando o paciente se encaixa nos critérios de eleição — as de Novartis e Janssen foram lançadas em 2022, e a Kite acaba de apresentar seu produto ao meio médico.
Pelos estudos clínicos e evidências de vida real, sabemos hoje que as CAR-T devolvem a perspectiva de remissão de um câncer a indivíduos que se viam antes num beco sem saída diante da doença.
Mas há um preço, literalmente. Só o tratamento, sem contar gastos com hospital, pode chegar a 2 milhões de reais.
Entre a empolgação e os desafios
Do primeiro paciente tratado com CAR-T no planeta, em 2010, até os dias atuais, muitas águas, células e inovações rolaram.
Na conferência europeia, especialistas já discutiam a terceira ou quarta geração da terapia, sem deixar de se ocupar também com os meios de torná-la mais barata e viável em larga escala.
De fato, ainda que sejam destinadas a uma fração do universo da oncologia, as CAR-T trazem resultados animadores.
No evento, Ulrich Jäger, professor de hematologia da Universidade Médica de Viena, na Áustria, destacou dois estudos com pacientes diagnosticados com quadros de linfoma folicular duros na queda.
Nessas análises, a taxa de sobrevivência foi de 75 a 88% dos casos em um período de dois a quatro anos após o procedimento. E boas notícias também vieram de pesquisas com outros tipos de linfoma, leucemia e mieloma múltiplo.
As CAR-T envolvem um processo de natureza bastante complexa — o que impacta o custo final do produto.
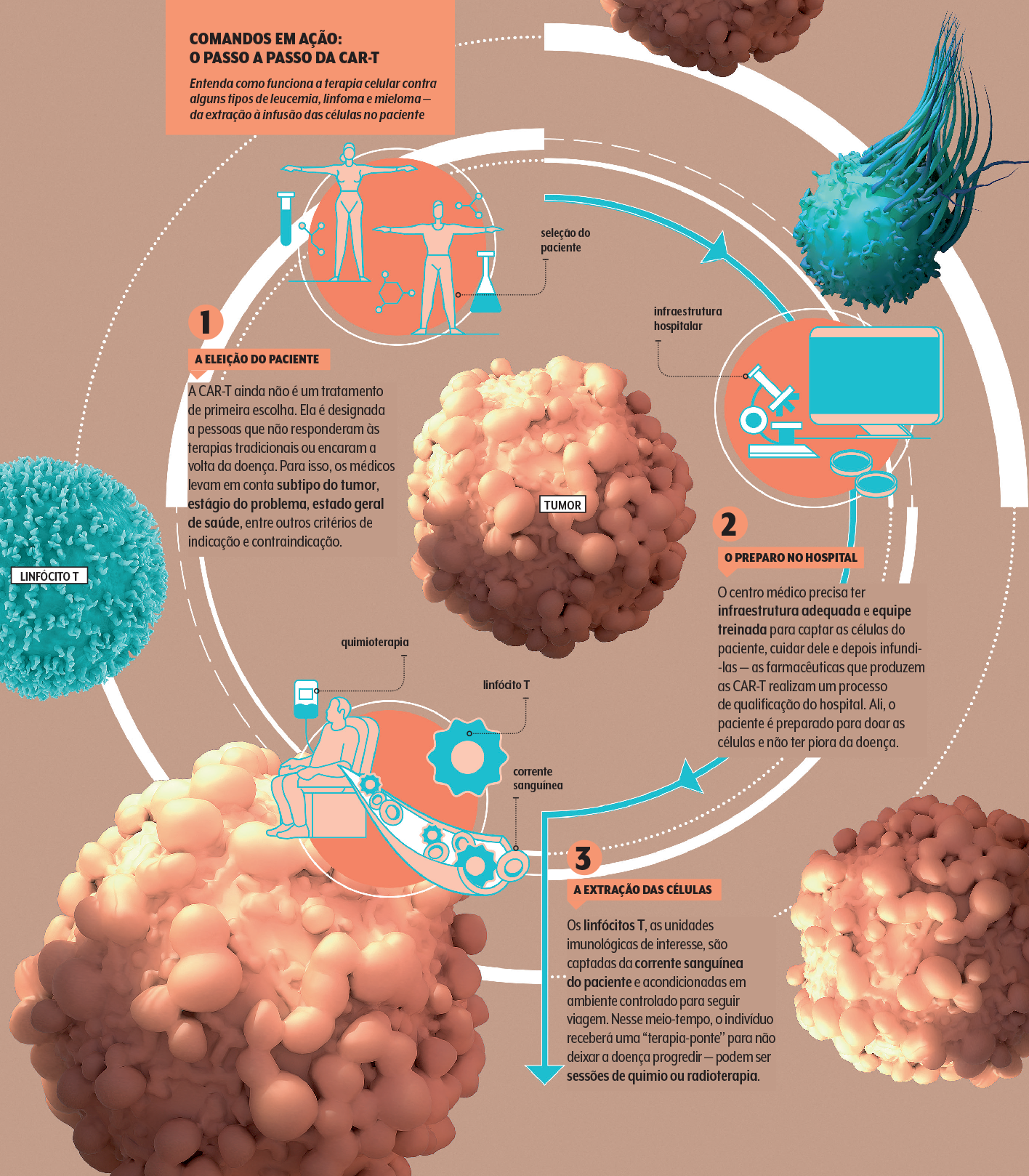
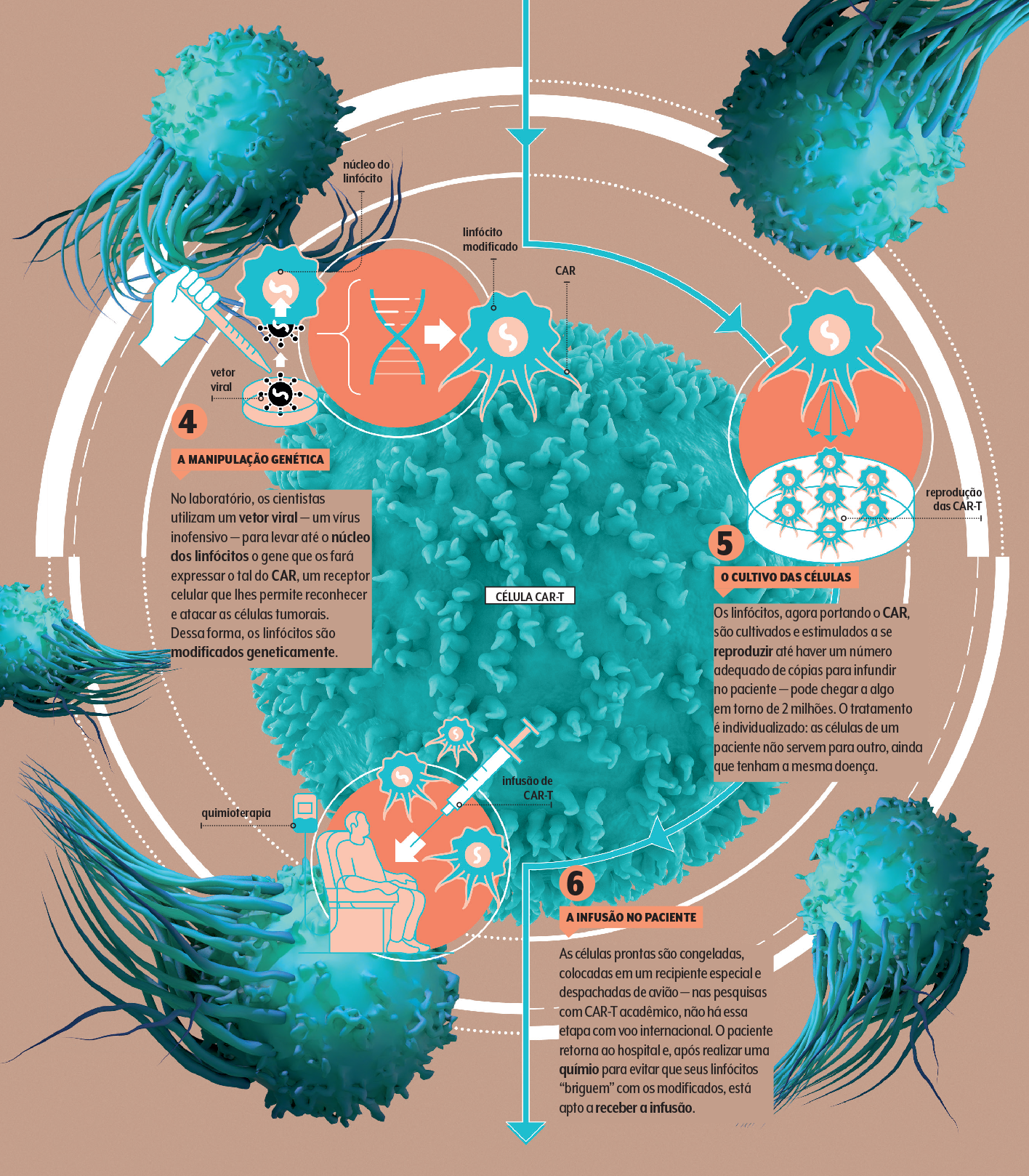
“A ideia é usar a engenharia genética para tornar células de defesa do paciente capazes de reconhecer e perseguir as células tumorais. O processo todo envolve a coleta dessas células, seu isolamento, modificação e cultivo em laboratório, e a infusão no paciente depois”, resume Harry Smith, diretor médico da Kite, empresa de biotecnologia que pertence à farmacêutica Gilead.
A Kite convidou VEJA SAÚDE a conhecer sua fábrica de CAR-T em Amsterdã, um dia antes de começar o congresso na Holanda. A instalação tem 19 mil metros quadrados, mais de 800 funcionários (de pelo menos 50 nacionalidades diferentes) e virou realidade após um investimento de 135 milhões de euros (quase 800 milhões de reais).
“Produzimos um lote individualizado por paciente, e isso leva entre 16 e 19 dias”, conta Marc Kamp, diretor de qualidade e um dos responsáveis pela operação fabril, pautada por protocolos rígidos, controle térmico e microbiano e zero emissão de carbono.
Quer dizer que é preciso “exportar” e “importar” as células de cada paciente? Isso mesmo. É uma das razões, aliás, que fazem com que o custo dessas terapias seja salgado no Brasil.
Primeiro, as farmas precisam qualificar um hospital para captar, da forma correta e sem risco de contaminação, os linfócitos (eis o nome dessas células).
Depois eles viajam para a Europa ou os EUA para serem manipulados geneticamente. Uma vez prontos, são reenviados ao país de origem, onde serão administrados ao indivíduo, que ficará uns dias internado para saber se está tudo ok.
A história toda pode levar alguns meses. Tecnologia de ponta, combustível para cruzar o oceano, assistência especializada… Doença complexa, solução complexa, processo complexo.
No Brasil, ainda poucos centros são capacitados a fornecer a CAR-T e o suporte necessário durante a jornada.
Um deles é o A.C.Camargo Cancer Center, na capital paulista, que investiu em infraestrutura e equipe para disponibilizar o tratamento. “Eu brinco que o treino acabou e agora começou o jogo pra valer”, diz o hematologista Jayr Schmidt, que coordena o setor.
Como em quase tudo que envolve medicina, a expectativa é que, com o tempo, o desenvolvimento e a expansão dessa área na oncologia, o preço dos procedimentos caia.
Mas uma alternativa para encurtar e agilizar o acesso aos pacientes é a pesquisa e produção de CAR-T dentro de universidades e hospitais nacionais.
Esse foi um dos tópicos levantados por Rocha em sua palestra no congresso europeu. O médico calcula que entre 1 800 e 2 200 brasileiros com leucemia e linfoma seriam candidatos a receber o novo tratamento por ano.
Hoje, porém, o número de pessoas tratadas dessa forma não passa da casa da dezena. A terapia não está no rol de cobertura dos convênios nem no SUS.
Por ora, fora do ambiente acadêmico, ou a família paga ou entra na Justiça para conseguir que o Estado ou o plano de saúde possam arcar com os gastos.
“Essas terapêuticas são promissoras e parecem revolucionárias, mas a questão da segurança e eficácia no longo prazo e o impacto financeiro são preocupantes para o sistema como um todo”, avalia Vera Valente, diretora-executiva da Federação Nacional de Saúde Suplementar (Fenasaúde).
Uma saída aventada a esse impasse é o modelo de compartilhamento de risco, em que o pagamento das operadoras ou do governo à farmacêutica se dá mediante os resultados da terapia na vida real — um jeito de dividir a conta.
+ LEIA TAMBÉM: Médico discute custo do câncer para a sociedade
Quem é candidato às CAR-T?
Nem todo caso de câncer pode ser tratado com a nova terapia — pelo menos até agora.
Ela se presta mais a alguns tipos específicos de tumores hematológicos, caso de linfomas de célula B, linfomas foliculares, leucemias linfoblásticas agudas e linfocíticas crônicas e mielomas múltiplos.
No geral, o uso da CAR-T é colocado em pauta quando dois ou mais tratamentos convencionalmente prescritos falham em controlar a doença ou quando ela acaba retornando mesmo depois dessas tentativas.
Ganha a ciência, ganha o paciente
Uma terceira via de acesso às CAR-T — e de forma gratuita — ocorre dentro de estudos clínicos ou em caráter de uso compassivo e experimental.
No A.C.Camargo, a equipe de Jayr Schmidt está realizando uma pesquisa para testar uma terapia celular comercial como uma abordagem mais inicial diante do mieloma múltiplo.
“Participar de um estudo é uma forma de o paciente ter acesso não só a medicamentos e procedimentos inovadores mas também a um acompanhamento que dificilmente ele teria de outra maneira, principalmente na rede pública”, ressalta o hematologista. É um ganha-ganha: a ciência ajuda o cidadão, e ele ajuda a ciência.
Não por menos, a Associação Brasileira de Hematologia, Hemoterapia e Terapia Celular (ABHH) acaba de lançar uma plataforma em seu site que reúne pesquisas em andamento e facilita a conexão entre pacientes, médicos e instituições.
Para viabilizar o acesso em maior escala, uma solução é o que os especialistas chamam de CAR-T acadêmico, aquele formulado e produzido nos domínios da universidade e dos centros públicos de pesquisa.
É um caminho promissor, que já vem sendo trilhado aqui e lá fora.
No congresso em Roterdã, o hematologista Álvaro Urbano-Ispizua, do Hospital Clínic Barcelona, na Espanha, compartilhou a bem-sucedida experiência catalã com uma versão própria de CAR-T, que custa um terço da opção comercial.
“Não podemos deixar os pacientes morrerem esperando pela terapia devido à dificuldade de acesso”, afirmou.
A USP e o Hemocentro de Ribeirão Preto colocam nosso país nesse mapa, e firmaram uma parceria com o Instituto Butantan para montar uma fábrica de terapia celular.
“A expectativa é que o valor do tratamento fique dez vezes mais barato que os comerciais”, prevê Rocha, que integra o grupo de estudos.
Um de seus pacientes, o Lucas citado no início da reportagem, é testemunha direta desse trabalho made in Brazil.
Diagnosticado com um tipo de leucemia no primeiro ano da faculdade, ele apresentou melhoras temporárias após um regime de quimioterapia e, mais tarde, o transplante de medula óssea. Só que a doença voltou com tudo.
“Chegou um momento em que os médicos me disseram que ou eu precisaria tentar um novo transplante ou a CAR-T, mas o custo dela era absurdo, inviável para minha família, até porque precisaria ir para fora do país”, recorda.
Lucas não queria passar pela odisseia de um novo transplante, um processo “pesado” e com inúmeras restrições. Ele queria se formar em medicina.
Rocha bolou, então, um esquema especial de quimioterapia, que, apesar dos efeitos colaterais, funcionou por um período. Só que, em menos de um ano, a doença voltou — de novo!
Porém, entrávamos em 2022 e, com a primeira CAR-T comercial em processo de aprovação por aqui, surgiu a oportunidade de Lucas testar, em caráter compassivo, a terapia celular bolada pela USP e o Hemocentro — ela já tinha funcionado contra o linfoma.
E deu certo! Lucas comenta que a terapia com a CAR-T, conduzida no Hospital das Clínicas de Ribeirão Preto, foi bem mais tranquila que o transplante de medula, pelo menos no seu caso.
Chegou a ir à UTI por precaução e ficou 15 dias no hospital para checar se não haveria nenhuma reação inesperada.
“Tive alta, e três dias depois já estava em Valença, no Rio, jogando um campeonato de vôlei com o time da faculdade”, relata.
“Eu ainda estava um pouco debilitado fisicamente, por ter ficado muito tempo parado, mas não só ganhamos o jogo como fui eleito o melhor jogador da partida”, celebra.
Nem todo paciente que passa por uma CAR-T tem essa sorte, cabe ponderar. “Estimamos que 40 a 50% delas precisam ficar na UTI. Quanto mais disseminado o tumor, maior a chance de complicações”, pontua Rocha.
Como em toda terapia complexa, pode haver eventos adversos. E por isso a infusão das CAR-T é feita em hospitais qualificados e credenciados para essa finalidade.
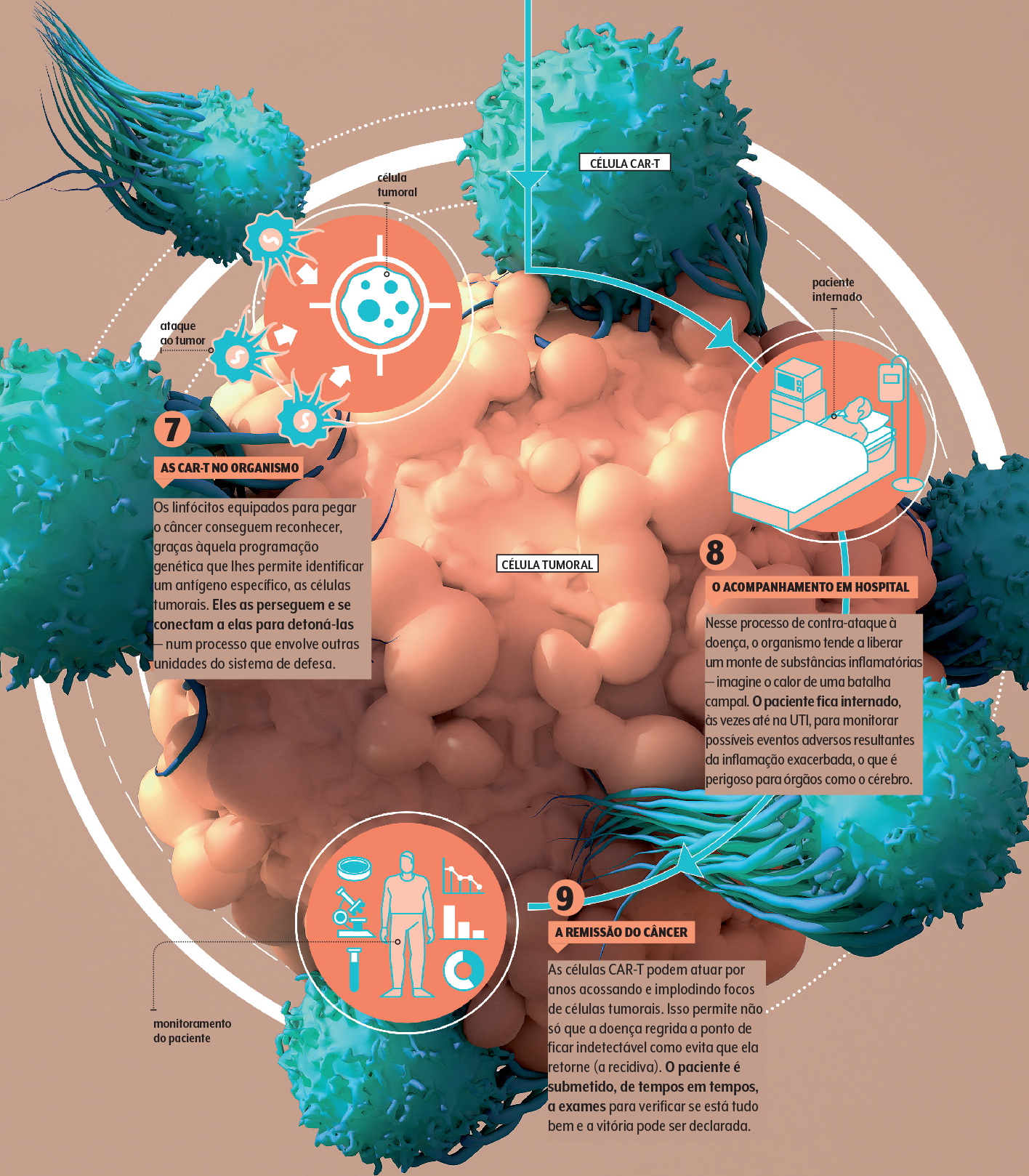
O hematologista Jayr Schmidt explica que é preciso monitorar e aplacar duas situações mais perigosas: uma reação inflamatória exagerada e sistêmica e a neurotoxicidade — a barreira natural que isola e defende o cérebro pode deixar de funcionar a contento, e moléculas indesejadas passam a perturbar o sistema nervoso.
Não é à toa que, segundo Rocha, uma das principais tendências debatidas no congresso europeu foi a busca por terapias cada vez mais eficazes e menos tóxicas.
+ LEIA TAMBÉM: A vanguarda dos tratamentos contra o câncer
Presente com um pé no futuro
Emily Whitehead completou uma década em remissão da leucemia. Lucas está prestes a fazer um ano livre do câncer.
Os médicos resistem a usar o termo “cura”, mas admitem que algo surpreendente acontece no organismo quando a terapia é bem indicada e funciona — ainda que sua efetividade possa cair ao longo do tempo.
Vejamos: um tumor só evolui porque o sistema de defesa não consegue mais freá-lo ou eliminá-lo. Então que tal dar uma mão a ele?
As CAR-T são um tipo de imunoterapia que convoca as células do paciente a contra-atacar o câncer. Elas passam por uma metamorfose e partem para a batalha devidamente equipadas. E o que acontece depois?
“Em alguns pacientes, esses linfócitos modificados já foram encontrados dez anos após a infusão. E os estudos começam a mostrar que a persistência dessa linhagem está associada a uma melhora na resposta clínica”, conta Lucila.
O que a hematologista do Einstein quer dizer com isso é que o risco de o câncer se levantar do nocaute (a recidiva, como preferem os experts) tende a diminuir sensivelmente.
De olho no dilema do acesso (sempre ele!) e nas perspectivas de aprimorar o tratamento em solo brasileiro, Lucila integra um projeto do Einstein, liderado pelo hematologista Nelson Hamerschlak, que irá avaliar o desempenho de uma terapia CAR-T desenhada inteiramente dentro da unidade de pesquisa do hospital paulistano. Coleta, engenharia genética, infusão, acompanhamento clínico…
Tudo acontece no mesmo ecossistema, numa iniciativa que faz parte do Programa de Apoio ao Desenvolvimento Institucional do Sistema Único de Saúde (Proadi-SUS), e, na primeira fase do estudo clínico, dará a oportunidade de pacientes da rede pública receberem cuidados de ponta.
Apesar dos desafios do presente, o Congresso Europeu de CAR-T trouxe um panorama empolgante: o das próximas gerações de terapia celular.
Sim, os cientistas não param e já quebram a cabeça para tornar o tratamento mais custo-efetivo, poder entrar em campo mais cedo, dar opção a quem não teve sucesso nem com ele (infelizmente, pode acontecer) e ampliar a lista de doenças beneficiadas.
Nos laboratórios já se investigam novos alvos moleculares para agregar às células de defesa modificadas, outras vias de edição genética dos linfócitos (hoje a preponderante é o vetor viral, em que um vírus inofensivo coloca a receita para a célula expressar o receptor desejado) e regimes combinados de CAR-T e com outras classes terapêuticas.
Carl June, o desbravador médico de Emily, falou de suas pesquisas com o que eles batizaram de TRUCK: células alteradas para reconhecer o antígeno que dedura o câncer mas também para interferir em um tipo de molécula inflamatória que participa desse processo.
Sua equipe vai comparar se o TRUCK (palavra em inglês para “caminhão”) é superior ao atual CAR (“carro”). Quem sabe a frota não irá crescer?
Mas e os tumores sólidos? As CAR-T não poderiam enfrentá-los também? Por ora, existem pesquisas incipientes tentando levar essa abordagem para a doença na próstata, na mama, no fígado…
Rocha explica que, para funcionar, a terapia celular precisa ter um antígeno (alvo) específico e funcional — como em alguns tipos de câncer hematológico — e os tumores sólidos impõem um desafio extra: as células modificadas têm de penetrar a massa tumoral.
Mas há estudos em curso, alguns com soluções inusuais, como juntar à CAR-T uma molécula do veneno de escorpião para atacar tumores cerebrais.
+ LEIA TAMBÉM: O que esperar do uso do ChatGPT na saúde?
Outro sonho no horizonte, e que já mobiliza pesquisadores, é o que o professor da USP chama de “terapia de prateleira”.
Imagine o seguinte: em vez de coletar, mudar e injetar células do paciente — processo que pode levar meses —, utilizar células prontas, de doadores saudáveis e manipuladas para bombardear tumores.
No Hemocentro de Ribeirão Preto, essa ideia está avançando e recebeu até uma premiação internacional. Lá, quem protagoniza os experimentos no laboratório da bióloga Virginia Picanço e Castro não são as CAR-T, mas as CAR-NK, outro tipo de célula de defesa capaz de identificar e combater o câncer (o NK vem de natural killers, “assassinas naturais”, no nosso idioma).
O futuro soa auspicioso. Sobretudo se investirmos em ciência. No encontro de Roterdã, o pai de Emily, Tom Whitehead, compartilhou seu trabalho à frente da fundação que leva o nome da filha e atua captando verbas para pesquisas e disseminando informação em prol da cura do câncer infantil. Sua missão é que outras meninas e meninos tenham a chance de se libertar da doença com uma terapia como as CAR-T.
Lucas tem uma meta parecida. Fazendo residência em clínica médica, ele quer se especializar em hematologia e cuidar de gente em situações semelhantes às que passou.
“Sou duplamente abençoado pela ciência. Como médico, que viu a medicina avançando a esse ponto. E como paciente, que teve a chance de receber um tratamento inovador que salvou minha vida”, diz.
Terapia celular: remédios vivos contra o câncer Publicado primeiro em https://saude.abril.com.br
Nenhum comentário:
Postar um comentário