Heitor nasceu prematuro, mas sem nada que chamasse a atenção dos médicos. Ficou na maternidade em João Pessoa alguns dias só para ganhar peso, e logo depois foi para casa. Numa consulta de rotina, porém, a pediatra notou que ele era muito paradinho, muito molinho. Não se movimentava bem. Os exames do pré-natal haviam sido normais, então a causa da hipotonia (falta de tônus muscular) era um mistério.
Seria uma reação aos remédios que a mãe tomava para a depressão pós-parto? Por via das dúvidas, a médica recomendou complementar a alimentação dele com fórmula (um tipo de leite em pó) e deixar Heitor pelo menos 24 horas no hospital em observação. Naquele mesmo dia, sem força para deglutir corretamente, o menino broncoaspirou (inalou) o leite. Teve de ser transferido para a UTI – de onde só saiu para outra, num hospital maior. E depois para mais uma. “Fomos migrando de hospital em hospital. Ao todo, Heitor ficou nove meses em UTI”, diz Hugo Moreira, pai do garoto.
Foi no meio dessa maratona que a família finalmente entendeu o que estava acontecendo. Heitor tem atrofia muscular espinhal (AME), uma doença genética rara, degenerativa e progressiva. Ela causa a perda dos neurônios motores, células do sistema nervoso que controlam o movimento dos músculos. Na ausência dessas células, os músculos se tornam cada vez mais fracos e atrofiam.
A criança não consegue sustentar a cabeça, engatinhar, sentar, andar nem falar. Conforme a doença evolui, ela passa a ter dificuldade para se alimentar e respirar, tendo de ser conectada a um respirador artificial. Os sintomas costumam se manifestar nos primeiros meses após o nascimento – e, antes do bebê completar o primeiro aniversário, a taxa de mortalidade é de 90%. Os que sobrevivem não costumam ir longe: a expectativa de vida para a AME tipo 1, a forma mais grave, não passa de dois anos.
Em suma, uma doença terrível. Ela tem tratamento: o Zolgensma, um medicamento lançado em 2019 pelo laboratório suíço Novartis. Basta uma única dose para fazer a AME regredir pelo resto da vida. E ele funciona em 97% dos casos. A má notícia é que se trata do remédio mais caro do mundo. A dose de Zolgensma custa inacreditáveis US$ 2,1 milhões – cerca de R$ 12 milhões pela cotação atual.
Ele quebrou todos os recordes, deixou médicos e cientistas perplexos e incendiou a polêmica sobre os preços praticados pela indústria farmacêutica. Qual é o critério para definir o preço de um medicamento? Qual é o máximo aceitável? Quanto vale uma vida? Enquanto a sociedade se debruça sobre essas questões, as famílias das crianças com AME correm contra o tempo para tentar conseguir o remédio.
A doença
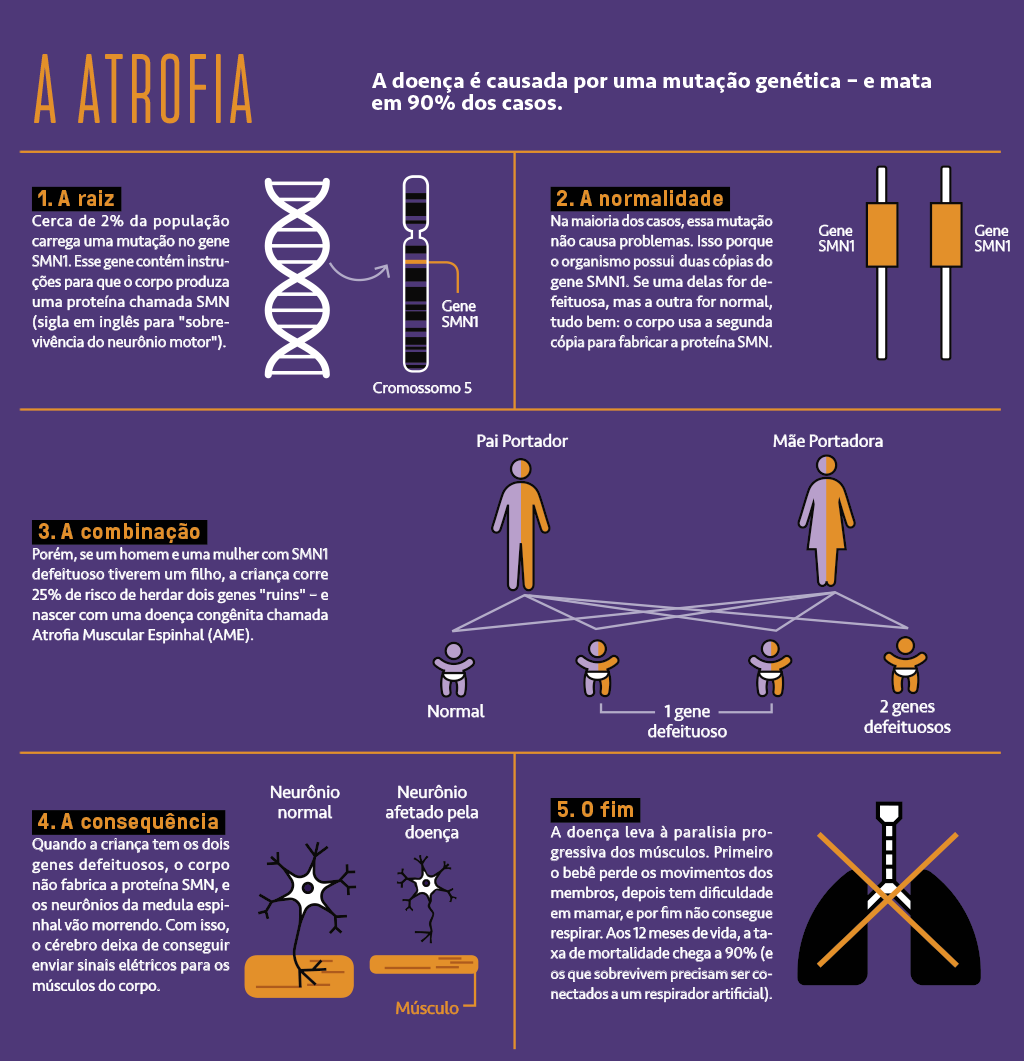
Apesar de rara, a AME é a principal causa genética de mortalidade infantil no mundo. Atinge 1 em cada 10 mil bebês, ou seja, em torno de 260 pessoas nascem com a doença no Brasil por ano. Ela é provocada por defeitos no SMN1, um gene que contém as instruções para que o organismo produza a proteína SMN (sigla em inglês para “sobrevivência do neurônio motor”). Quando o corpo não fabrica a proteína SMN, ou faz isso em quantidade insuficiente, os neurônios motores – que ficam dentro da medula espinhal e levam sinais do cérebro para os músculos – vão definhando. E a vítima vai perdendo os movimentos do corpo.

A AME costuma passar despercebida no nascimento. Isso porque, no Brasil, o “teste do pezinho” atualmente oferecido pelo SUS só rastreia seis doenças genéticas, como hipotireoidismo congênito, fenilcetonúria e fibrose cística. Uma lei aprovada em maio amplia esse número para 50, mas a rede pública tem um ano para implementar a mudança, que ocorrerá de forma escalonada. A AME só será incluída na quinta e última etapa.
Até lá, muitas famílias enfrentarão a mesma maratona de Heitor. “Essa história se repete: os pais notam que o filho está um pouco paradinho, alguém desconfia, um médico examina, depois outro, o bebê faz tomografia, ultrassonografia, raio X… e ninguém descobre nada”, diz Hugo, o pai. “Heitor é o nosso primeiro filho, e não há nenhum caso de AME na família. Não tinha nem como imaginar que existisse essa possibilidade.”
Os genes são segmentos de DNA que ficam armazenados no interior dos cromossomos. Cada gene tem duas versões, os alelos. Você herda um alelo do seu pai e o outro da sua mãe. Alguns alelos são dominantes, ou seja, definem sozinhos uma determinada característica física. É o caso do gene OCA2, que determina a cor dos olhos. Se você herdar o alelo “B” do seu pai ou da sua mãe, terá olhos castanhos, não importando qual for o outro alelo. Já os olhos azuis são recessivos: só acontecem se houver uma combinação de dois alelos “b” (formando a dupla “bb”).
A AME é uma doença recessiva. Isso significa que, para tê-la, o bebê precisa herdar a mutação em ambas as cópias do gene SMN1. Aproximadamente 2% da população possui uma única cópia defeituosa do gene. São os chamados “portadores”, que não desenvolvem a doença. Mas se dois portadores se casarem e tiverem um filho, ele terá 25% de chance de herdar ambas as mutações, e ter AME [veja infográfico abaixo].
O diagnóstico da doença é confirmado com testes genéticos, que determinam se há mutação no gene SMN1. O problema é que o acesso a esses exames também não é fácil. A família de Heitor foi informada de que a análise genética levaria três meses. Enquanto isso, a doença avançava rápido. “A gente se desesperou e veio para Recife, que tem uma rede hospitalar mais bem preparada. Estamos aqui há oito meses”, diz o pai. (No dia da entrevista, Heitor estava com 1 ano e 8 dias e morava no Recife desde os 4 meses de vida.)
Quando finalmente conseguem o diagnóstico, as famílias iniciam uma etapa ainda mais difícil: o acesso ao tratamento.
O remédio
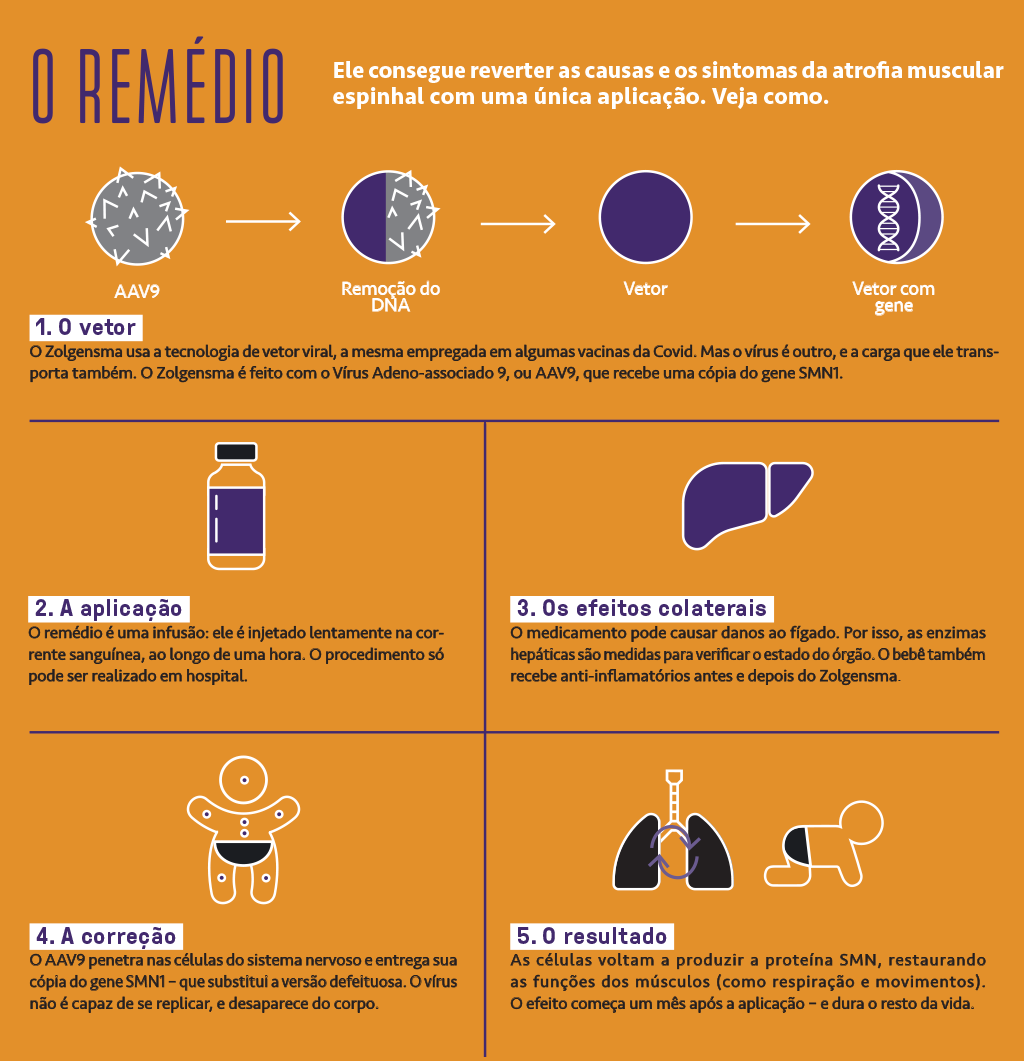
A AME não tem cura. Mas o Zolgensma pode reverter a doença – pois consegue substituir o gene SMN1 defeituoso por uma cópia normal. Ele usa a tecnologia de vetor viral, a mesma empregada em algumas das vacinas contra Covid.
O medicamento contém um adenovírus geneticamente modificado, o AAV9, que é injetado na corrente sanguínea do paciente e se espalha pelo corpo, inundando o organismo com uma versão sadia do gene – a dose, que é calculada de acordo com o peso do bebê, contém mais de 300 trilhões de unidades dele.

Algumas chegam à medula espinhal, e são incorporadas pelos neurônios motores. Como esses neurônios não se replicam ao longo da vida, o conserto está feito – eles passam a usar o gene correto, conseguem fabricar a proteína SMA, e os sintomas da doença começam a regredir. (O vírus-vetor não se reproduz, e é eliminado do organismo.) A vida da criança está salva – e ela pode começar o longo processo de fisioterapia para recuperar os movimentos.
Foi assim com a menina Helena, de Santo Antônio do Descoberto (Goiás), que recebeu o remédio com 1 ano e 2 meses de vida. Dois dias após a aplicação, a mãe dela já começou a perceber diferença. “Antes de receber o Zolgensma, a Helena parecia uma boneca que a gente colocava na cama e ficava ‘largadona’. Não mexia”, diz Neicy Ferreira. “Hoje, com 1 ano e 5 meses, ela movimenta mais as mãos, consegue mexer a cabeça, segurar as perninhas e firmar o pescocinho e o tronco.”
A parte respiratória também melhorou. Helena ficava 24 horas por dia conectada a um respirador artificial, e agora já consegue passar alguns minutos sem, durante a fisioterapia. “A Helena que eu vi há oito meses era totalmente diferente da que eu vejo hoje. É como se eu tivesse dado à luz de novo. É uma nova vida”, diz a mãe.
Neicy conta como foram os primeiros sinais da doença. “Com 20 dias de nascida, coloquei a Helena na minha barriga e ela estava bem durinha, mexendo os pezinhos e as mãozinhas. Só fui achar estranho a partir dos três meses, pois ela não conseguia mais mamar. Ficava como se estivesse engasgando. Eu achava que ela não queria mais meu leite e comecei a dar fórmula”, afirma.
Helena também começou a ficar molinha. Quando ela completou quatro meses, a mãe tentou colocá-la sentada mas não conseguiu. “Lembrei que meu filho mais velho já sentava e rolava na cama nessa idade. Vi que alguma coisa estava errada. Então a coloquei sobre minha barriga, como fiz quando ela tinha 20 dias. Mas ela caía”, diz.
O quadro respiratório piorou e a menina foi internada. A família passou por diversos médicos e exames, até que um geneticista explicou que havia suspeita de AME. “Eu não queria acreditar. Pelo que o médico falou, minha filha podia morrer a qualquer momento”, diz Neicy. Dois meses depois, Helena teve uma parada cardiorrespiratória em casa. “Ela ficou roxa. Achei que ela não ia passar dali, mas consegui socorrê-la e levá-la ao hospital”, diz Neicy. Helena obteve o Zolgensma pelo SUS graças a uma ação na Justiça, numa batalha que costuma ser árdua (mais sobre isso daqui a pouco).
O Zolgensma é um enorme avanço em relação aos outros tratamentos para a AME, como o medicamento Spinraza (lançado em 2016 pelo laboratório americano Biogen). Lembra do gene SMN1, que faz o corpo produzir a proteína SMN, essencial para a sobrevivência dos neurônios? Pois bem: existe um outro gene, chamado SMN2, que funciona como um quebra-galho. Se o corpo não tem o SMN1, ou ele é defeituoso, o organismo apela para o SMN2 – ele produz uma proteína um pouco mais curta, que não funciona tão bem quanto a completa.
É aí que entra o Spinraza: ele modifica o gene SMN2, permitindo que fabrique a proteína completa. Mas há vários poréns. Enquanto o Zolgensma é de dose única, o Spinraza precisa ser aplicado durante toda a vida. A criança inicialmente toma três “doses de ataque”, com intervalo de 14 dias, e uma quarta dose 30 dias mais tarde. A partir daí, precisa receber uma dose do medicamento a cada quatro meses.
Outra diferença é que o Spinraza deve ser administrado por via intratecal (uma injeção diretamente na medula espinhal, na parte inferior das costas), num procedimento que pode ser arriscado. Já o Zolgensma é aplicado numa veia do braço ou da perna, o que é bem mais simples e seguro.
E o mais importante: o Spinraza desacelera a progressão da doença, mas não impede que ela continue avançando. Heitor tomou cinco doses do Spinraza e teve melhoras no desenvolvimento motor, mas não tanto na respiração. Também começou a perder a capacidade de sorrir, o que apavorou a família. O Spinraza não é tão caro quanto o Zolgensma, mas também custa uma fortuna: cerca de R$ 320 mil a dose.
A longo prazo, a despesa pode acabar até maior, já que o medicamento deve ser usado por toda a vida (a um custo de R$ 960 mil por ano). O Spinraza é oferecido gratuitamente pelo SUS. Mas isso nem sempre é cumprido; em alguns casos, as famílias também tiveram de entrar na Justiça para conseguir recebê-lo.
A polêmica
A Novartis não desenvolveu o Zolgensma; comprou da AveXis, uma farmacêutica que ela adquiriu em 2018 por US$ 8,7 bilhões. Em maio de 2019, o medicamento foi aprovado pela FDA (a Anvisa dos EUA) para uso em crianças de até 2 anos, e chegou ao mercado americano. Mas, logo após o sinal verde da FDA, surgiram evidências de que a AveXis havia omitido ou distorcido dados envolvendo a toxicidade do Zolgensma em ratos de laboratório. A data da morte dos animais, ou seja, quanto tempo eles sobreviveram após receber o remédio, estava incorreta. Essa diferença chegava a 19 dias, fazendo o medicamento parecer menos tóxico do que realmente era.

Uma investigação da FDA revelou que a AveXis sabia da irregularidade desde março de 2019, mas só informou a agência sobre ela em 28 de junho – mais de um mês após a liberação do Zolgensma. O caso gerou escândalo nos Estados Unidos, mas a FDA decidiu não punir o fabricante. “Nossas preocupações no momento são limitadas a apenas uma pequena parte dos dados de teste do produto”, declarou a agência (1). “Esses dados não alteram a avaliação positiva sobre as informações dos ensaios clínicos em humanos.”
Ainda assim, a FDA afirmou que teria adiado sua decisão se soubesse dos problemas antes, para poder investigar mais a fundo os estudos de toxicidade em animais. A Novartis reconheceu o erro, mas publicou uma nota em que reitera a segurança do remédio, citando “evidências que demonstram a eficácia do produto e seu perfil de segurança”, com relação “risco/benefício favorável.” (2)
Em agosto de 2020, a Anvisa liberou o Zolgensma no Brasil, também para menores de 2 anos. “Os efeitos colaterais do produto são considerados controláveis, sendo que o mais comum observado nos estudos foi o aumento das enzimas hepáticas, resolvido após tratamento com corticosteroides”, afirmou a agência (3).
Um estudo realizado nos EUA com 100 bebês revelou que, em 90% dos casos, eles tinham níveis aumentados das enzimas hepáticas (4), o que pode indicar danos no fígado. Isso acontece porque, ao detectar a presença do vírus AAV9, o organismo dispara uma reação imunológica contra ele – e as células de defesa acabam atacando o fígado. Mas, na maioria dos casos, essa reação pode ser contida com anti-inflamatórios. E considerando a alternativa, que é não usar o Zolgensma e deixar a AME evoluir para uma morte quase certa, o “perfil de segurança” dele de fato parece bastante aceitável.
O Zolgensma sobreviveu à “pedalada” da AveXis. Mas tinha pela frente outra tempestade: a controvérsia envolvendo seu preço.
A loteria e os milhões
Por que o Zolgensma custa exatos US$ 2,1 milhões e não outro valor qualquer, como 1, 3 ou 5 milhões – cifra que chegou a ser cogitada pela Novartis durante o desenvolvimento do medicamento? Qual é o critério para definir isso? A empresa diz que levou em conta três fatores ao estipular o preço: o ganho terapêutico oferecido pelo remédio, seu mecanismo de ação único (que atua diretamente na causa da doença, não apenas sobre os sintomas) e o processo de produção da droga, que é caro e complexo.
São argumentos válidos, mas há nuances envolvidas. O remédio usa um vetor viral (um adenovírus montado em laboratório para transportar determinado pedaço de material genético), mesma tecnologia usada nas vacinas anti-Covid da AstraZeneca e da Johnson & Johnson, bem como na russa Sputnik V. E elas custam 5 a 10 dólares a dose; não US$ 2 milhões.
É que existe uma diferença de escala. Enquanto essas vacinas terão centenas de milhões, ou até bilhões, de doses fabricadas e vendidas, o Zolgensma vai vender muito menos – simplesmente porque não existem bilhões de crianças com AME, precisando dele. Dessa forma, o investimento inicial feito pela empresa farmacêutica precisará se pagar com um número muito menor de tratamentos (e eles serão caros).
A Novartis também argumenta que, como seu medicamento é de dose única, ele acaba sendo mais barato do que outros tratamentos genéticos. “Se usarmos como exemplo medicamentos incorporados ao SUS que já estão há mais de dez anos no mercado para outras doenças genéticas, como as mucopolissacaridoses (5), cuja expectativa de vida dos pacientes é de 40 anos, pode-se extrapolar que o custo total poderia chegar a R$ 87 milhões durante toda a vida do paciente”, disse a empresa à Super.
Uau. Oitenta e sete milhões de reais. Esse é um exemplo extremo, pinçado pela Novartis para fazer o remédio dela parecer menos caro. Mas os altos preços dos medicamentos são um problema clássico da indústria farmacêutica, que vive nadando em dinheiro – só nos EUA, o setor faturou impressionantes US$ 535 bilhões em 2020 (um crescimento de 4,9% em relação ao ano anterior).
A pandemia de Covid-19 contribuiu para esse aumento, mas o principal motivo foram os “medicamentos especiais”, hipercaros, que tratam doenças raras, genéticas ou complexas. A despesa com eles está crescendo depressa, e pode ultrapassar 50% de todo o gasto com remédios nos EUA já este ano, segundo projeção da Sociedade Americana de Farmacêuticos (6).
Os laboratórios dizem que cobram caro pelos remédios porque precisam de dinheiro para desenvolver novas drogas, um processo que pode levar décadas (e no qual mais de 90% das substâncias avaliadas acabam fracassando). É verdade. Mas há outro fator envolvido. O grupo americano PharmacyChecker analisou os relatórios financeiros de 2019 de cinco das maiores empresas do setor: Novartis, Pfizer, GSK, Eli Lilly e AbbVie. Em todos os casos, as empresas haviam gastado mais em marketing e promoção de vendas do que em pesquisa e desenvolvimento (P&D). A Novartis, que naquele ano teve uma receita de US$ 34,2 bilhões, gastou US$ 9,4 bilhões em P&D e US$ 14,3 bilhões em marketing e vendas (7).
Isso desfaz a imagem de abnegação científica que a indústria farmacêutica gosta de projetar, e pode ser um pouco antipático – mas não é ilegal. A Novartis, assim como os outros laboratórios, tem o direito de gastar mais em marketing, se achar adequado. Porém, no caso específico do Zolgensma, há um complicador: o desenvolvimento inicial da droga teve dinheiro público. Ao longo das últimas duas décadas, o National Institutes of Health (NIH) do governo americano investiu mais de US$ 35 milhões em pesquisas com adenovírus na Universidade da Pensilvânia (8), onde o vetor AAV9 foi criado, testado – e, depois, licenciado pela AveXis.
Está longe de ser o único caso do tipo (mais de 40 empresas licenciaram patentes de adenovírus criados na universidade), e também não tem nada de irregular. Mas mostra que os laboratórios farmacêuticos nem sempre inventam tudo aquilo o que comercializam. Às vezes, eles simplesmente têm o faro para pescar inovações no meio acadêmico – e fazer dinheiro em cima.
Bota dinheiro nisso. As 25 maiores empresas farmacêuticas do mundo operam com margem de lucro de 22%, em média, muito acima de qualquer outro setor da economia (9) (é quase o dobro da média de lucratividade empresarial nos EUA, 13%). Analistas de Wall Street estão prevendo que as vendas do Zolgensma cheguem a US$ 2 bilhões no ano que vem, segundo uma pesquisa da empresa de dados financeiros Refinitiv.
A Novartis doa 100 doses do Zolgensma por ano no mundo, numa loteria um pouco polêmica (a intenção é boa, mas não deixa de ser macabro submeter famílias a um sorteio que pode definir a sobrevivência ou morte do bebê). Segundo a empresa, para participar da loteria, os bebês precisam ter menos de 2 anos de idade, diagnóstico de AME e morar em países onde o tratamento ainda não tem aprovação regulatória. No Brasil, uma criança foi beneficiada pela iniciativa. Mas a loteria não é mais válida por aqui. “Como o produto já tem registro no país, o Brasil automaticamente deixou de ser elegível”, afirma a Novartis.

O valor cobrado pelo remédio, US$ 2,1 milhões, é o praticado no mercado internacional. No Brasil, o Zolgensma ainda não tem preço oficial, tabelado, e por isso está sujeito a outro fator: a cotação do dólar, que disparou nos últimos dois anos. “A gente tem conseguido que o laboratório pratique uma taxa cambial menor, fazendo com que o valor do Zolgensma caia para R$ 9 milhões”, diz a advogada Daniela Tamanini, que assessora famílias de crianças com AME.
Também há outro problema: o imposto. Alguns Estados brasileiros, como Paraíba e Distrito Federal, já têm leis que isentam o ICMS do medicamento. Assim, com R$ 9 milhões a família consegue importá-lo. Em outros Estados, é cobrado imposto, o que encarece o produto. “Famílias que moram na Paraíba pagam cerca de R$ 9 milhões pelo remédio, por exemplo, enquanto as que moram em Goiás gastam quase R$ 12 milhões”, cita Tamanini.
Isso é especialmente absurdo porque, na maioria das vezes, quem paga o remédio é o próprio governo, por meio do SUS, que tem sido obrigado na Justiça a custear o tratamento. É o caso de Rafael Pelincário, de Bom Jesus do Galho (MG). O menino recebeu o diagnóstico de AME em dezembro de 2020, quando tinha 1 ano e meio.
A família arrecadou R$ 4 milhões em doações e em maio conseguiu na Justiça que o Governo Federal pagasse o resto. Mas a decisão não foi cumprida imediatamente; e a doença continuava a avançar rápido. Em 21 de julho, Rafael finalmente recebeu o remédio. “Ele já teve grandes evoluções, como firmar a cabecinha, mexer as perninhas, firmar o tronco e ter mais força nas mãos”, diz o pai, Adriano.
A família de Heitor Moreira passou pela mesma angústia. Venceu na Justiça, mas a União recorreu, alegando que não há comprovação científica que o Zolgensma seja melhor que o Spinraza. A família também entrou com uma ação contra o plano Saúde Caixa (Hugo, pai do garoto, é gerente da Caixa Econômica). Em março, a Justiça ordenou que a Caixa pagasse R$ 6 milhões (a família havia conseguido o resto em doações).
Mas a Caixa entrou com recurso, argumentando que o valor era muito alto e poderia quebrar o plano de saúde. “Essa não é uma justificativa plausível nem dentro da moral, porque você não pode botar um preço na vida de uma pessoa”, diz Tamanini. “A Constituição não fala que você só pode ser atendido pelo plano de saúde até R$ 1 milhão, por exemplo.” Em 19 de agosto, Heitor conseguiu o remédio. “Ele já segura a cabeça e fica quase o dia todo sem a máscara do respirador”, diz Hugo, o pai.
Tamanini estima que nove crianças já tenham recebido o Zolgensma no Brasil. Uma delas obteve o remédio na loteria da AveXis, duas ou três conseguiram com campanha de arrecadação; e as demais via Justiça. O caso da menina Kyara Lis, do Distrito Federal, foi o mais emblemático: Tamanini entrou com mandado de segurança diretamente no Superior Tribunal de Justiça (STJ) contra o ministro da Saúde.

Essa ação audaciosa deu certo, entre outras coisas, porque a família tinha uma documentação muito extensa e conseguiu arrecadar mais de R$ 5 milhões em doações, cabendo ao Ministério da Saúde pagar o restante. “Como a decisão veio do STJ, foi cumprida dentro do prazo estipulado. Mas, com todas as outras decisões das outras crianças, é sempre uma luta: sai a decisão, a União não paga. Eles ficam enrolando o máximo que conseguem para não cumprir a decisão”, diz a advogada.
O raciocínio por trás disso é tão claro quanto sórdido. Como a AME avança depressa, há enormes chances de que a criança morra se não receber o medicamento – o que eliminaria a despesa com a compra dele. É uma lógica cruel, mas que ilustra bem um fato da vida: a medicina não acontece no vácuo, apartada das fraquezas humanas.
Ela é feita por pessoas, existe dentro de uma sociedade, e portanto está sujeita à ganância e ao egoísmo – dois males infinitos, que matam tanta gente quanto as doenças mais terríveis. Mas que, assim como elas, não são impossíveis de curar.
***
Fontes
(1) Statement on data accuracy issues with recently approved gene therapy. FDA, 2019. (2) Novartis stands behind Zolgensma for the treatment of children less than 2 years of age with spinal muscular athropy. 2019. (3) Aprovado registro de produto de terapia gênica. Anvisa, 2020. Disponível em bit.ly/3Ef84EB. (4) Hepatotoxicity following administration of onasemnogene abeparvovec (AVXS-101) for the treatment of spinal muscular atrophy. D Chand e outros, 2020. (5) Doença que causa má-formação do esqueleto e problemas neurológicos.(6) National trends in prescription drug expenditures and projections for 2021. E Tichy e outros. (7) www.pharmacychecker.com/askpc/pharma-marketing-research-development (8) NIH Reporter Tool. Pesquisa disponível em bit.ly/3BdYxfc. (9) www.globaldata.com/top-25-global-pharma-companies-market-cap-end-2017
O remédio mais caro do mundo Publicado primeiro em https://super.abril.com.br/feed
Nenhum comentário:
Postar um comentário